|

|
Sempre que falamos em "radiação", as
pessoas logo fazem "cara feia", "torcem o nariz" em
uma manifestação de uma espécie de receio, ou até
mesmo por medo em relação ao que essa palavra
significa. Porém, estas pessoas provavelmente não
sabem que estão
constantemente
expostas aos mais diversos tipos de radiação,
desde as consideradas "naturais" até aquelas
"artificiais". Dentre as "naturais", podemos
destacar a denominada
radiação de
fundo,
sendo que os seus principais geradores são o
radônio, raios cósmicos e nucleotídeos presentes no
corpo (ex. carbono 14, potássio-40)
Sem dúvida, a radiação é um fenômeno
interessantíssimo, com diversas aplicações nas mais
diversas áreas do conhecimento. Na arqueologia, a
análise de compostos emissores de radiação tornou-se
uma ferramenta muito importante na determinação de
dados sobre a idade, tanto de matéria viva ou não,
em especial, seres vivos que a muito tempo habitaram
a Terra. O método proposto por
Willard F.
Libby
(veja foto ao lado) para usar a radiação do carbono
14 na datação foi muito importante para a
arqueologia avançar nos seus conhecimentos sobre o
passado.
Denomina-se radioatividade a atividade que
certos átomos possuem de emitir radiações
eletromagnéticas e partículas de seus núcleos
instáveis com o propósito estabilizarem-se.
Admite-se que a estabilidade de um núcleo esteja
relacionada com a relação entre o número de prótons
e nêutrons, de forma que: |
|
Há mais de 50 anos era descoberta a técnica
de datação pelo carbono 14 |
|
 |
Ganhador do premio Nobel de Química em 1960,
Willard F. Libby foi o cientista que,
em 1949, na revista Science, publicou
um artigo sobre a datação com radiocarbono.
Três anos depois, ele registrara em seu
livro Radiocarbon Dating baseada no
carbono 14 - elemento essencial na
composição dos organismos vivos. |
|
Libby nasceu em Grand Valley,
Colorado, em 17 de dezembro de 1908. Ele
era um Físico-Químico especialista em
radiochemistry, química de átomo
particularmente instáveis. Ficou famoso na
Universidade de Chicago para o trabalho dele
em natural carbono-14 (radiocarbon) e seu
uso datando artefatos arqueológicos, e
tritium (isótopo do Hidrogênio) natural,
e seu uso em hidrologia e geofísica.
Saiba mais sobre o cientista consultando o
site do prêmio Nobel:
http://www.nobel.se/chemistry/laureates/1960/ |
|
|

|
Com
exceção do hidrogênio, que é um elemento
estável mesmo sendo destituído de nêutrons,
os elementos entre o hélio (42He)
e e cálcio (4020Ca)
são muito estáveis e possuem, na relação de
prótons e nêutrons o valor igual a 1. Á
medida que a relação assume valores maiores,
a estabilidade começa a ser comprometida e,
quanto atinge-se o número de 83 prótons no
núcleo, nenhum número de nêutrons é capaz de
neutralizá-lo. O bismuto, (Z = 83) é o
último elemento da tabela periódica que
possui isótopo estável, 20983Bi.
A
datação por radiocarbono, ou carbono-14
No
início da década de 1990, um cadáver de
homem pré-histórico foi encontrado numa
geleira próxima à fronteira entre a Itália e
Áustria. Seu estado de conservação era
espantoso (havia provavelmente sido
desidratado por ventos frios antes de
congelar). Os cientistas usaram o método do
carbono-14 para determinar que sua morte
ocorreu há cerca de 5.300 anos. Mas a
questão é: porque? |
relembrando...
A massa atômica ou a massa de um átomo é
dada pela seguinte relação:
A = Z + N
sendo
A = massa do átomo*
Z = número atômico, que é igual ao número de
prótons do núcleo,
N = número de nêutrons
* Perceba que o núcleo atômico é responsável
praticamente por toda a massa do átomo,
tendo em vista que a massa do elétron e
comparação ao próton, por exemplo, é 1836
vezes menor. |
|
|
Essa pergunta nos remete a uma análise de
como o carbono-14, radioativo, é formado e porque
ele é utilizado na datação. Vamos analisar a
abundancia dos três isótopos de carbono existente na
natureza.
|
Isótopo |
Abundância
Natural |
Radioativo? |
|
126C |
98,9% |
Não |
|
136C |
1,1% |
Não |
|
146C |
0,000001% |
Sim |
|
Os
raios cósmicos
(ver mais sobre ao lado), que vem do
espaço sideral, atravessam a atmosfera
terrestre e arrancam nêutrons dos átomos
do ar. Os nêutrons têm uma meia-vida
curta (certa de 13 min); a 17 km de
altitude a concentração de nêutrons é
máxima; na superfície da Terra, porém,
chega a apenas 2,4 nêutron/cm².s. Com o
oxigênio do ar os nêutrons não reagem;
com o nitrogênio porém há reação:

Forma-se assim o carbono-14, radioativo
(ver relação próton/nêutron) e de
meia vida muito longa (5.600 anos).
Na atmosfera o carbono-14 se "queima",
transformando-se em CO2, que
é absorvido pelos vegetais (no processo
de fotossíntese) e daí passa para os
animais. |
O que são raios cósmicos?
Os raios cósmicos são partículas
sub-atômicas, com velocidades próximas à
da luz (300.000 km/s), que preenchem
todo o espaço cósmico e eventualmente
atingem a Terra.
Qual a composição dos raios cósmicos?
Os raios cósmicos galáticos são
compostos aproximadamente de:
> 90% de prótons (núcleo do átomo de
hidrogênio)
> 7% de partículas alfa (núcleo do átomo
de Hélio)
> 1% de núcleos de Carbono, Nitrogênio e
Oxigênio (no. atômico entre 6-8)
>1% de elétrons e pósitrons (antipartícula
do elétron)
> 0,01% de raios gama (fótons de alta
energia)
>0,0001% de núcleos de elementos pesados
A composição dos raios cósmicos
primários reflete, ainda que
aproximadamente, a composição do
Universo. A composição dos raios
cósmicos solares é diferente e
relacionada à abundância relativa dos
elementos no Sol.
Fonte: Projeto Microsul - UFSC
http://server.fsc.ufsc.br/~canzian/rcosmicos/ |
|
Partindo do pé-suposto que a quantidade
de carbono-14 manteve-se constante nos
últimos 20.000 anos, o teor de
carbono-14 também é constante nos
vegetais e animais,
enquanto vivos
(cerca de 15 desintegrações por minuto e
por grama de carbono total). |
No entanto,
quando o vegetal ou animal morrem, cessa a absorção
de CO2 com carbono radioativo, e começa o
decaimento do carbono-14, de acordo com a equação:
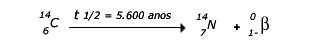
Esse
decaimento, assim, após 5.600 anos, a radioatividade
cairá para a metade. Desse modo, medindo a
radioatividade residual do fóssil, podemos calcular
a sua idade. A grande dificuldade está no fato de
essa radioatividade ser muito fraca; são
necessários, então contadores de grande precisão e,
ainda por cima, isolados da influência dos raios
cósmicos. que chegam constantemente à superfície da
Terra. Com esses cuidados, podemos efetuar datações
de até 40.000 anos, com erros da ordem de 200 anos.
|
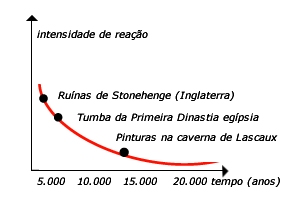
Na caverna
de Lascaux (França) foram encontradas
pinturas do homem pré-histórico, que,
por análise do carbono 14, revelaram ter
aproximadamente 16.000 anos.
 |
Entendendo o conceito de meia vida com
um exemplo doméstico
Um
exemplo caseiro pode apresentar, de
forma simples, o conceito de meia-vida:
uma família de 4 pessoas tinha 4 kg de
açúcar para seu consumo normal.
Logicamente, a função do açúcar é adoçar
o café, o refresco, bolos e sucos.
Adoçar é a atividade do açúcar, assim
como a emissão de radiação é a atividade
dos elementos radioativos.
Por
haver falta de açúcar no supermercado,
foi preciso fazer um racionamento, até a
situação ser normalizada, da seguinte
forma: na primeira semana, foram
consumidos 2 kg, metade da quantidade
inicial, e conseguiu-se. fazer dois
bolos, um pudim, refrescos, sucos, além
de adoçar o café da manhã. Na segunda
semana, foi consumido 1 kg, metade da
quantidade anterior e ¼ da inicial. Aí,
já não deu para fazer os bolos.
Na
terceira semana, só foi possível adoçar
os refrescos, sucos e café, com os 500
gramas então existentes.
Procedendo da mesma forma, na décima
semana restaram cerca de 4 g de açúcar,
que não dariam para adoçar um cafezinho.
Essa quantidade de açúcar não faria mais
o efeito de adoçar e nem seria
percebida. No exemplo citado, a
meia-vida do açúcar é de uma semana e,
decorridas 10 semanas, praticamente não
haveria mais açúcar, ou melhor, a
atividade adoçante do açúcar não seria
notada. No entanto, se, ao invés de 4
kg, a família tivesse feito um estoque
de 200 kg, após 10 meias-vidas, ainda
restaria uma quantidade considerável de
açúcar.
Se o
racionamento fosse de sal, a meia-vida
do sal seria maior, por que a quantidade
de sal que se usa na cozinha é muito
menor do que a de açúcar. De fato,
leva-se muito mais tempo para gastar 4
kg de sal do que 4kg de açúcar, para uma
mesma quantidade de pessoas
(consumidores).
fonte: Apostila educativa:
Radioatividade - CNEN Comissão Nacional
de Energia Nuclear
http://www2.cnen.gov.br/ensino/apostilas/radio.pdf |
 |
A massa do
neutrino e suas conseqüências
Um imenso detector construído no
interior de uma antiga mina, no Japão,
obteve as primeiras evidências de que as
partículas elementares denominadas
neutrinos, o contrário do que se
acreditava, têm massa.
Os neutrinos são produzidos em reações
no interior das estrelas e na atmosfera
terrestre. A cada segundo, bilhões
passam através do nosso corpo sem que
percebemos, pois eles interagem muito
pouco com a matéria.
O
Superkamiokande, um detector neutrinos
instalado sob uma montanha japonesa, a
um custo de U$$ 100 milhões, consiste em
um tanque da altura de um edifício de
oito andares, contendo 50 mil toneladas
de água. Alguns poucos neutrinos, entre
os bilhões que passam sem interagir,
colidem com átomos da água e, em geral,
quando ocorre uma colisão, um elétron é
atirado para longe em altíssima
velocidade. Essa é a vantagem do grande
tanque: na água, esse elétron veloz
emite radiação (a chamada radiação de
Cherenkov), facilmente medida. Através
da medição os físicos podem calcular
quantos neutrinos de cada tipo passam
pelo tanque durante certo intervalo de
tempo.
Fonte:
Revista Ciência Hoje, n° 142, fevereiro
de 1999, p.20. |
|
|