 Embora
possam existir "zilhões" de substâncias químicas
diferentes, elas são combinações de pouco mais de uma
centena de elementos químicos. Um elemento
químico é qualquer substância que não pode ser
decomposta em outras substâncias mais simples através de
processos químicos ordinários: os elementos são os
tijolos fundamentais com os quais toda a matéria é
feita. Dos 116 elementos químicos conhecidos, cerca de
20% não existe na natureza: foram preparados
sinteticamente em laboratórios. Os elementos químicos
podem se combinar e formar substâncias mais complexas,
chamadas de compostos, que possuem características
diferentes dos elementos que o constitui. Por exemplo,
dois átomos do elemento Hidrogênio e um átomo do
elemento Oxigênio podem se combinar e formar uma
molécula de água (H2O). A
água em nada se assemelha aos gases oxigênio e
hidrogênio. Embora
possam existir "zilhões" de substâncias químicas
diferentes, elas são combinações de pouco mais de uma
centena de elementos químicos. Um elemento
químico é qualquer substância que não pode ser
decomposta em outras substâncias mais simples através de
processos químicos ordinários: os elementos são os
tijolos fundamentais com os quais toda a matéria é
feita. Dos 116 elementos químicos conhecidos, cerca de
20% não existe na natureza: foram preparados
sinteticamente em laboratórios. Os elementos químicos
podem se combinar e formar substâncias mais complexas,
chamadas de compostos, que possuem características
diferentes dos elementos que o constitui. Por exemplo,
dois átomos do elemento Hidrogênio e um átomo do
elemento Oxigênio podem se combinar e formar uma
molécula de água (H2O). A
água em nada se assemelha aos gases oxigênio e
hidrogênio.
Os filósofos gregos Tales, Anaximenes e Heráclitos, muito
antes de Cristo, foram os primeiros a sugerir a composição
elementar da matéria: Thales achava que o elemento
fundamental era a água; Anaximenes dizia que era o ar e
Heráclitos acrediva que era o fogo.
 Um
outro filósofo grego, Epédocles, disse que todas as
substâncias eram compostas de 4 elementos: água, fogo, terra
e ar. Aristóteles também pensava assim, e inclusive atribuiu
as propriedades físicas das substâncias como derivação das
propriedades elementares. Embora pareça estranho, o
pensamento grego já trazia os fundamentos da química
moderna: falava-se em elementos, compostos, substâncias...
Demócrito e Lêucipo, em torno de 400 anos A.C., criaram o
termo "átomo"
(do grego, "indivisível") para descrever o que, na sua
concepção, seriam as unidades elementares da matéria. Um
outro filósofo grego, Epédocles, disse que todas as
substâncias eram compostas de 4 elementos: água, fogo, terra
e ar. Aristóteles também pensava assim, e inclusive atribuiu
as propriedades físicas das substâncias como derivação das
propriedades elementares. Embora pareça estranho, o
pensamento grego já trazia os fundamentos da química
moderna: falava-se em elementos, compostos, substâncias...
Demócrito e Lêucipo, em torno de 400 anos A.C., criaram o
termo "átomo"
(do grego, "indivisível") para descrever o que, na sua
concepção, seriam as unidades elementares da matéria.
 Em
1661, o químico inglês Robert Boyle estabeleceu a
diferença entre elemento e substância e, em 1789, o químico
francês Antoine-Laurent Lavoiser publicou o que pode
ser considerada a primeira lista de elementos baseada nas
definições de Boyle. Nesta lista estavam citados "sílica" e
"alumina", entre outros, que hoje sabemos se tratar de
substâncias, e não elementos. Em
1661, o químico inglês Robert Boyle estabeleceu a
diferença entre elemento e substância e, em 1789, o químico
francês Antoine-Laurent Lavoiser publicou o que pode
ser considerada a primeira lista de elementos baseada nas
definições de Boyle. Nesta lista estavam citados "sílica" e
"alumina", entre outros, que hoje sabemos se tratar de
substâncias, e não elementos.
Mesmo os antigos já conheciam 7 dos elementos químicos
(ouro, prata, chumbo, ferro, mercúrio, zinco e cobre), sendo
citados mesmo na Bíblia. Os outros elementos foram
descobertos a partir da segunda metade do século 18, quando
as técnicas de separação e caracterização foram aprimoradas.
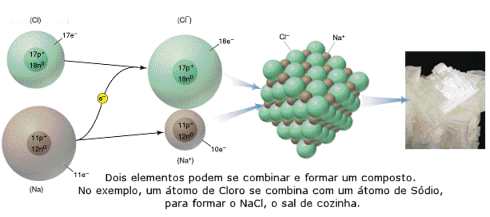

No exemplo acima, o Potássio reage com o Cloro para formar
KCl.
|
O ano da descoberta dos Elementos
|
|
Até o ano 1 A.D. |
Au |
Ag |
Cu |
Fe |
Pb |
Sn |
Hg |
S |
C |
|
Alquimistas
1 A.D. to 1735 |
As |
Sb |
Bi |
P |
Zn |
|
|
|
|
|
|
1735-1745 |
Co |
Pt |
|
|
|
|
|
|
|
|
|
1745-1755 |
Ni |
|
|
|
|
|
|
|
|
|
|
1755-1765 |
|
|
|
|
|
|
|
|
|
|
|
1765-1775 |
H |
N |
O |
Cl |
Mn |
F |
|
|
|
|
|
1775-1785 |
Mo |
W |
Te |
|
|
|
|
|
|
|
|
1785-1795 |
U |
Sr |
Ti |
Y |
|
|
|
|
|
|
|
1795-1805 |
V |
Cr |
Be |
Nb |
Ta |
Ce |
Pd |
Rh |
Os |
Ir |
|
1805-1815 |
Na |
K |
Ba |
Ca |
Mg |
B |
I |
|
|
|
|
1815-1825 |
Li |
Cd |
Se |
Si |
Zr |
|
|
|
|
|
|
1825-1835 |
Al |
Br |
Th |
|
|
|
|
|
|
|
|
1835-1845 |
La |
Tb |
Er |
Ru |
|
|
|
|
|
|
|
1845-1855 |
|
|
|
|
|
|
|
|
|
|
|
1855-1865 |
Cs |
Rb |
Tl |
In |
|
|
|
|
|
|
|
1865-1875 |
|
|
|
|
|
|
|
|
|
|
|
1875-1885 |
Ga |
Yb |
Sm |
Sc |
Ho |
Tm |
|
|
|
|
|
1885-1895 |
Pr |
Nd |
Gd |
Dy |
Ge |
Ar |
|
|
|
|
|
1895-1905 |
He |
Eu |
Kr |
Ne |
Xe |
Po |
Ra |
Ac |
Rn |
|
|
1905-1915 |
Lu |
|
|
|
|
|
|
|
|
|
|
1915-1925 |
Hf |
Pa |
|
|
|
|
|
|
|
|
|
1925-1935 |
Re |
|
|
|
|
|
|
|
|
|
|
1935-1945 |
Tc |
Fr |
At |
Np |
Pu |
Cm |
|
|
|
|
|
1945-1955 |
Md |
Fm |
Es |
Am |
Pm |
Bk |
Cf |
|
|
|
O Portal de Estudos em Química
apresenta um pouco de história.
Na tabela ao lado, o ano da descoberta de cada
elemento químico. Na tabela abaixo, alguns exemplos
que justificam por quê alguns símbolos não tem,
aparentemente, nenhuma relação com o nome do
elemento. E, em seguida, dois novos elementos
químicos.
Nome em Português
|
Símbolo
|
Nome Original |
Antimônio
|
Sb
|
Stibium
|
Cobre
|
Cu
|
Cuprum
|
Ouro
|
Au
|
Aurum
|
Ferro
|
Fe
|
Ferrum
|
Chumbo
|
Pb
|
Plumbum
|
Mercúrio
|
Hg
|
Hydragyrum
|
Potássio
|
K
|
Kalium
|
Prata
|
Ag
|
Argentum
|
Sódio
|
Na
|
Natrium
|
Estanho
|
Sn
|
Stannum
|
Tungstênio
|
W
|
Wolfram
|
|
|
arquivo://Novos
Elementos: 118 e
116
|
|
Dois
novos elementos foram descobertos
(ou criados?)
pelo grupo de cientistas liderado por
Ken Gregorich, no Lawrence
Berkeley National Laboratory, na
Califórnia.
|
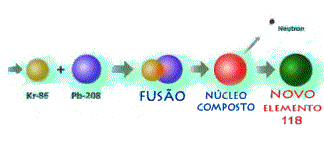
No 88-Inch Cyclotron,
os cientistas aceleraram íons de kriptônio-86 a
energias da ordem de 449 milhões de elétrons-volt.
Este fluxo de íons foi colidido contra uma população
de chumbo-208. Os elementos 118 e 116 são
extremamente instáveis, e sua existência só pode ser
confirmada pela análise de seus produtos de
decaimento radioativo. A interpretação dos
resultados, indicou que o 86Kr e 208Pb se fundiram
em um elemento transitório 118 (massa atômica
de 293 com 175 nêutrons). Em menos de 1 milisegundo,
este elemento decaiu para formar uma partícula alfa
(2 prótons e 2 nêutrons) e um átomo do elemento
116 (massa atômica 289 com 173 nêutrons).
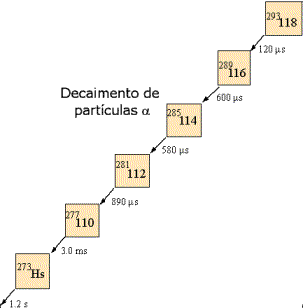
Eliminações sucessivas de partículas alfa resultaram
nos elementos 114, 110, 108 e 106.
I-Yang Lee, diretor
científico do 88-Inch Cyclotron, resumiu a
importância deste experimento: "From the
discovery of these two new superheavy
elements, it is now clear that the island
of stability can be reached.
Additionally, similar reactions can be used
to produce other elements and isotopes,
providing a rich new region for the study of
nuclear and even chemical properties."
|
43 technetium (1936)
85 astatine (1940)
93 neptunium (1940)
94 plutonium (1940)
95 americium (1944)
96 curium (1944)
97 berkelium (1949)
98 californium (1950)
99 einsteinium (1952)
100 fermium (1952)
101 mendelevium (1955)
102 nobelium (1958)
103 lawrencium (1961)
104 ruterfordium (1969)
105 hahnium (1970)
106 seaborgium (1974)
116 sem nome (1999)
118 sem nome (1999) |
Estes não
foram os primeiros elementos a serem
descobertos no Lawrence Berkeley National
Laboratory.
Confira, ao lado, a lista dos elementos
descobertos (nomes em inglês) neste
laboratório. |
 |
|
|