
Bolhas de ar, cristais de
gelo e glóbulos de gordura: não há quem não adore!
Todos nós somos doidos por sorvetes, uma das mais
gostosas invenções da humanidade.
Embora possa ser
encontrado em qualquer esquina, o sorvete é um
verdadeiro fenômeno químico: diversas fases
heterogêneas que, macroscopicamente, formam uma
deliciosa massa homogênea e cremosa.
|
 Uma
coisa é certa, e todos concordamos: sorvete é
gostoso. Mesmo o imperador romano Nero, no século IV antes
de Cristo, era um adepto: costumava enviar soldados até as
montanhas para conseguir neve - misturando sucos de frutas,
neve e mel, Nero tinha um protótipo do que hoje chamamos de
sorvetes. Dentre as várias novidades trazidas pelo
aventureiro Marco Polo quando foi para a China, estavam
várias receitas de sorvetes - e isto foi antes de 1300! Uma
coisa é certa, e todos concordamos: sorvete é
gostoso. Mesmo o imperador romano Nero, no século IV antes
de Cristo, era um adepto: costumava enviar soldados até as
montanhas para conseguir neve - misturando sucos de frutas,
neve e mel, Nero tinha um protótipo do que hoje chamamos de
sorvetes. Dentre as várias novidades trazidas pelo
aventureiro Marco Polo quando foi para a China, estavam
várias receitas de sorvetes - e isto foi antes de 1300!
 Entretanto,
foi somente lá pelo século XVII que o sorvete passou a ser
feito sem o auxílio da neve; com a descoberta de que
o sal pode abaixar a
temperatura de fusão da água o advento da
fabricação do sorvete surgiu. Já por volta de 1800, vários
restaurantes e cafés da Europa, principalmente na França,
passaram a oferecer sorvetes no seu menu. E, em 1851, a
primeira fábrica de sorvete, em Baltimore, foi fundada.
Poucos anos depois, a refrigeração mecânica (os freezers)
foram introduzidos, e sorveterias se proliferaram pelo mundo
inteiro. Entretanto,
foi somente lá pelo século XVII que o sorvete passou a ser
feito sem o auxílio da neve; com a descoberta de que
o sal pode abaixar a
temperatura de fusão da água o advento da
fabricação do sorvete surgiu. Já por volta de 1800, vários
restaurantes e cafés da Europa, principalmente na França,
passaram a oferecer sorvetes no seu menu. E, em 1851, a
primeira fábrica de sorvete, em Baltimore, foi fundada.
Poucos anos depois, a refrigeração mecânica (os freezers)
foram introduzidos, e sorveterias se proliferaram pelo mundo
inteiro.
 Embora
mais coloridos, com formas diversas e bizarras, os
ingredientes básicos que estão num sorvete atual continuam
muito parecidos com aqueles feitos na antiguidade.
Quem já fez sorvete em casa
provavelmente usou gemas de ovos, leite, creme de leite e
açúcar, assim como frutas ou suco destas para dar o aroma.
Nas grandes fábricas, o sorvete é feito com gordura,
proteínas, água, leite, açúcar, estabilizantes e
emulsificantes. Não há, de fato, grandes diferenças em
relação à composição do "home-made" sorvete. Embora
mais coloridos, com formas diversas e bizarras, os
ingredientes básicos que estão num sorvete atual continuam
muito parecidos com aqueles feitos na antiguidade.
Quem já fez sorvete em casa
provavelmente usou gemas de ovos, leite, creme de leite e
açúcar, assim como frutas ou suco destas para dar o aroma.
Nas grandes fábricas, o sorvete é feito com gordura,
proteínas, água, leite, açúcar, estabilizantes e
emulsificantes. Não há, de fato, grandes diferenças em
relação à composição do "home-made" sorvete.
Um alerta: não se deixe enganar pela simplicidade dos
ingredientes. A mera
existência do sorvete já é uma ameaça aos conceitos
fundamentais da química. Num bom sorvete, gotas
de gordura, bolhas de ar e cristais de gelo são igualmente
dispersos em uma espessa solução de açúcar para formar a
matriz semi-sólida, congelada e aerada que conhecemos. O
impossível acontece e é maravilhoso.
|
O sorvete visto de perto: SEM & TEM
|
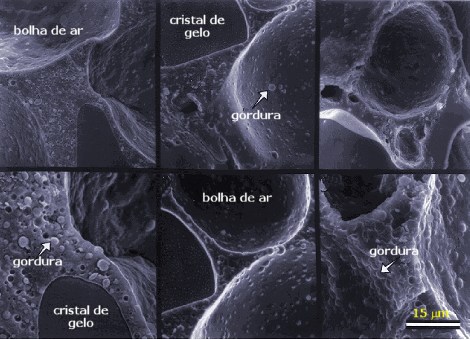
Na imagem acima, obtida pela técnica de
microscopia de varredura eletrônica
(SEM), podemos observar, dispersos na
solução de açúcar, as várias fases do
sorvete: bolhas de ar, glóbulos de gordura e
os cristais de gelo.
Através de outra técnica, mais poderosa (TEM,
microscopia de transmissão eletrônica)
somos capazes de ver até as micelas de
caseína. Repare, na figura abaixo, como as
micelas sempre ficam próximas aos glóbulos
de gordura.

Fonte: International Dairy
Journal 9 (1999) 817-819 |
|
Fazer o sorvete "dar certo" é uma arte.
Se você colocar os ingredientes acima em um liquidificador,
bater e depois levar ao freezer irá obter uma meleca:
enormes placas de gelo envoltas em um creme irregular e
desuniforme. Para fazer o sorvete com um freezer, a mistura
deve ser agitada manualmente e, mesmo durante o
resfriamento, continuamente. Somente a agitação regular pode
evitar a formação de grandes cristais de gelo. Agora, se
você for um químico, a tarefa pode ser muito mais simples:
basta misturar os ingredientes ainda quentes e jogar uma boa
quantidade de nitrogênio líquido. Instantaneamente, o
sorvete (de ótima aparência) fica pronto. Uma boa forma de
impressionar seus amigos, não é?! O nitrogênio líquido
esfria a mistura tão rapidamente que não há tempo para
grandes cristais de gelo se formarem, criando um sorvete
fino, cremoso e homogêneo. Parte do nitrogênio, na forma de
gás, é aprisionado dentro da mistura, fazendo o sorvete
ficar particularmente aerado. Perfeito, em apenas 30
segundos.
Água e óleo não se misturam, certo?! Errado - o próprio
leite já é uma emulsão de
gordura em água (leia quadro ao lado). No leite,
a gordura é aprisionada em
membranas protéicas, sob a forma de glóbulos.
Estes glóbulos são bastante estáveis no leite, mas esta não
é uma qualidade desejada para o sorvete: para formar um bom
sorvete, estes glóbulos devem colapsar, ou seja, devem ser
menos estáveis. Para isto, os fabricantes adicionam
emulsificantes
(surfactantes), como mono ou di-glicerídeos, que diminuem a
tensão superficial dos glóbulos, permitindo a formação da
emulsão coloidal. Para quem não lembra ou faltou às aulas de
química no segundo grau, um sistema coloidal é definido como
um sistema que tem um ou mais componentes com um tamanho
variando de um nanômetro a um micrômetro em pelo menos uma
dimensão. Se agitarmos uma mistura de água, óleo e
surfactante teremos uma emulsão coloidal.
Efeito da adição de
emulsificantes nas estruturas dos glóbulos de
gordura, usando Cryo-SEM
 Como visto na figura, o aumento da concentração
de emulsificante faz com que mais glóbulos de
gordura possam ser vistos na interface com o ar,
ou seja, uma maior interpenetração da gordura
nas bolhas de ar - uma qualidade ideal para a
estabilidade do sorvete. Isto também é
importante para a retenção da
forma do sorvete com o aumento da temperatura,
como visto na figura abaixo:
Como visto na figura, o aumento da concentração
de emulsificante faz com que mais glóbulos de
gordura possam ser vistos na interface com o ar,
ou seja, uma maior interpenetração da gordura
nas bolhas de ar - uma qualidade ideal para a
estabilidade do sorvete. Isto também é
importante para a retenção da
forma do sorvete com o aumento da temperatura,
como visto na figura abaixo:
 Fonte: International Dairy Journal 10 (2000)
303-309
Fonte: International Dairy Journal 10 (2000)
303-309
|
Entretanto, para fazer com que o sorvete não colapse e ainda
tenha derrete-na-boca características,
as concentrações de mono- e
diglicerídeos precisam ser meticulosamente selecionadas.
Se forem muito altas, os glóbulos de gordura colapsam em
grandes blocos gordurosos, fazendo o sorvete parecer uma
manteiga. O sorvete deve permanecer por horas a 4
o C, num processo chamado envelhecimento,
onde os glóbulos são estabilizados e a viscosidade da
emulsão aumenta, devido à hidratação dos emulsificantes.
O próximo passo envolve a
desestabilização em um SSHE (scraped-surface heat
exchanger), que simultaneamente congela e promove a aeração
da mistura. Isto muda drasticamente as propriedades do
sorvete: cristais de gelo começam a crescer e bolhas de ar
são inseridas na emulsão. Os fabricantes evitam o
supercrescimento dos cristais de gelo através de grandes pás
rotatórias, que quebram os cristais em pedaços menores do
que 50 micrômetros. A aeração é muito eficaz:
um sorvete regular contém
mais de 50% de ar! Sem isto, a textura de um
sorvete não seria tão diferente de um cubo de gelo, e daria
uma péssima impressão ao paladar. Um quadro abaixo ilustra a
importância de uma boa aeração.
O ar no sorvete é um tema constante de pesquisas
químicas.
Mais que um desafio para os cientistas, é uma arte para os
fabricantes. As bolhas devem ser pequenas e uniformes,
finamente dispersas. Se colapsarem, saem da mistura e o
sorvete não retém mais sua forma. De uma maneira geral, as
bolhas de ar não podem ter mais do que 100 micrômetros de
diâmetro. Se forem maiores, o sorvete derrete muito
rapidamente.
Aí entram as proteínas:
são elas que estabilizam as bolhas de ar e os glóbulos de
gordura! A principal é justamente a caseína, uma proteína
micelar, abundante no leite. São as micelas de caseína que
ficam em volta dos glóbulos de gordura, tornando-os estáveis
dentro da emulsão. E os sacarídeos e polissacarídeos
presentes também têm um papel importante: solúveis na água,
impedem esta de congelar completamente, pois diminuem o
ponto de fusão do líquido. O resultado é uma viscosa
solução, que faz com que o sorvete seja macio - e não duro
como um iceberg! Esta solução saturada de sacarose é chamada
de plasma ou serum. Num bom sorvete, o serum está sempre no
estado líquido.
|
Efeito do
tempo de agitação na aeração do sorvete
|
|
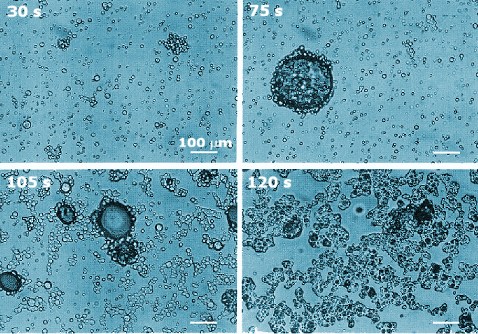
Na aeração, o creme é batido juntamente com o ar. O
tempo é um fator importante; na primeira figura, com
apenas 30s de agitação, as grandes bolhas de ar
escapam da mistura, restando apenas pequenas bolhas
na emulsão. Após 75s de agitação já observa-se a
existência de bolhas maiores. A melhor situação
parece ocorrer a 105s, onde os glóbulos de gordura e
as bolhas de ar estão bem dispersos na emulsão e
bastante estáveis. Se o tempo for maior, como vemos
na foto a 120s, há demasiada coalescência dos
glóbulos de gordura, formando grandes fases
gordurosas. O gráfico abaixo ilustra o efeito da
agitação durante a aeração sobre vários parâmetros
do servete.

Fonte: Colloids and Surfaces A 190 (2001) 333-354 |
|
Sorvete com cobertura |
 Como
é feito a cobertura de chocolate ou de sucos no
sorvete? Como
é feito a cobertura de chocolate ou de sucos no
sorvete?
Utilizando banhos sucessivos de nitrogênio líquido,
os fabricantes são capazes de desenvolver uma
"casca" de chocolate ou de suco no sorvete de
palito. Devido ao aprisionamento de micro-bolhas de
ar entre as camadas de cobertura, o resultado é um
sorvete crocante.
Clique no sorvete ao lado para ver uma animação.
|
Somente após a saída do SSHE é que
o sorvete recebe os
ingredientes finais: sucos ou aromas artificiais
de frutas, com o sabor requerido, além de corantes e outros
aditivos. No caso de pedaços de frutas ou castanhas, o
cuidado é especial: estes elementos são tratados
quimicamente antes de serem adicionados, pois podem carregar
bactérias e outros contaminantes, capazes de destruir a
emulsão. O sorvete, então, é armazenado em temperaturas
inferiores a -30 o C; acima de 25
o C os cristais de gelo continuam a
crescer e as bolhas de ar se expandem.
Alguns modelos de sorvete vêm
com uma cobertura de chocolate ao redor. O
processo para fabricação destes sorvetes não é muito
complicado, e envolve o uso de nitrogênio líquido, conforme
descrito no quadro ao lado.
Agora, na primavera, os consumidores vão começar a comprar
toneladas de sorvetes nos supermercados e outros
estabelecimentos. O que você acha, todavia, que os
fabricantes estiveram fazendo durante o inverno? Obviamente,
fizeram estoques de sorvetes, de todos os sabores. Mas há um
problema: os sorvetes não são estáveis com o passar do
tempo. Entram em campo,
novamente, os químicos.
|
Efeito do emulsificante na estabilidade
|
% mono- e diglicerídeo |
0 |
0.075 |
0.15 |
0.15 |
0.15 |
0.15 |
|
% polisorbato 80 |
0 |
0 |
0 |
0.02 |
0.04 |
0.06 |
|
taxa de derretimento (%min
-1 ) |
0.9 |
1.0 |
0.8 |
0.2 |
0.2 |
0.1 |
A taxa de derretimento foi medida à 20
o C
Fonte: International Dairy Journal 10 (2000)
303-309 |
Há várias formas de monitorar a estabilidade de um sorvete.
Uma delas é a medida da
taxa de derretimento: os químicos colocam o
sorvete sobre uma grade, dentro de uma cabine de temperatura
controlável. Cada pingo que cai do sorvete passa pela grade
e é coletado em uma balança, embaixo. Várias composições são
testadas (e.g. variando as concentrações de proteínas,
emulsificantes, tempo de aeração, etc.) até que o sorvete
passe por este teste. A microscopia de varredura eletrônica
também é uma ferramenta muito popular nesta área, pois
permite uma visualização em escala microscópica da mistura.
Hoje, milhões de toneladas de sorvete são consumidas
anualmente, quer seja nos países quentes ou frios. Além de
ser um bom negócio, o sorvete também é um vasto campo de
pesquisa para os químicos: a ciência está sendo convidada a
participar das várias etapas da fabricação do sorvete.
Parece uma área de pesquisa
vantajosa: se no final do expediente os resultados não forem
bons, o químico ainda pode, ao menos, comer parte de suas
amostras...
|
|
Got Milk?!
|
 O
leite tem sido usado como alimento pelos humanos desde os
tempos mais remotos. Inicialmente, o leite era consumido
in natura, tal como saia do animal; hoje, dispomos do
leite pasteurizado e podemos encontrar a versão whole,
low-fat ou skim. Não obstante, diversos
derivados do leite (dairy products) são consumidos no
mundo inteiro, como queijos, iogurtes, sorvetes e leite
condensado. O
leite tem sido usado como alimento pelos humanos desde os
tempos mais remotos. Inicialmente, o leite era consumido
in natura, tal como saia do animal; hoje, dispomos do
leite pasteurizado e podemos encontrar a versão whole,
low-fat ou skim. Não obstante, diversos
derivados do leite (dairy products) são consumidos no
mundo inteiro, como queijos, iogurtes, sorvetes e leite
condensado.

De longe, o leite extraído de vacas é o mais consumido por
humanos, mas este não é o único animal. Além da vaca,
consumimos leite de búfalos (principalmente na Índia, China,
Egito e Filipinas), cabras (nos países mediterrâneos), renas
(norte da Europa) e ovelhas (sul europeu). O leite de vaca
não é o mais nutritivo; entretanto, o alto consumo deste
leite está associado ao frequente manejo bovino (por causa
da carne) e ao grande volume de leite produzido por estes
animais: em 1800, a média anual de produção láctea de uma
vaca era de de 1500 litros. Hoje, graças a uma melhor
nutrição e refinamento das raças, uma única vaca é capaz de
fornecer 10.000 litros de leite/ano! A campeã é a
Holstein-Friesian; entretanto, vacas das raças
Ayirshire, Guernsey e Brown Swiss produzem
um leite mais rico em gorduras e proteínas.
Nossa primeira refeição, ao nascer, é o leite: como todos os
mamíferos, somos capazes de produzir o leite para amamentar
nossos filhotes. Além de ser um alimento, o leite materno
também contém uma boa dose de anticorpos - é uma verdadeira
vacina. Entretanto, não somos os únicos animais que
apreciamos o leite mesmo quando adultos: gatos, cachorros e
praticamente qualquer outro animal também comem leite,
sempre que tiverem uma chance...

A grande maioria das pessoas classificaria o leite como
sendo uma bebida. Entretanto, esta classificação é
equivocada: enquanto um tomate ou uma folha de alface, por
exemplo, contém apenas 6% de sólidos, no leite esta
quantidade ultrapassa 13%. Desta maneira, o leite deve ser
considerado um alimento, e não uma bebida. Dentre todos os
leites, o mais nutritivo é o extraído das renas: contém mais
de 36% de sólidos (10% de proteínas e 22% de gorduras). Este
leite é um dos melhores para o preparo de queijos.
O leite é uma suspensão, e não uma solução: nele, partículas
dispersas são estabilizadas na fase liquida. Os maiores
componentes são água, gorduras, proteínas, carbo-hidratos e
minerais. Entretanto, embora em menor quantidade, outros
componentes são igualmente importantes, como vitaminas e
aminoácidos essenciais. Mais de 250 substâncias químicas
diferentes já foram identificadas no leite bovino.
Na lista abaixo, podemos ter uma ideia da composição geral
do leite.
Composição do leite
De uma forma geral, o leite bovino é uma mistura de varias
substâncias, entre elas:
>87 % água
>13 % de sólidos, sendo:
# 4 % gordura
# 3.25% proteínas (3/4 caseína)
# 4.6% lactose
>minerais 0.65% - Ca, P,
Mg, K, Na, Zn, Cl, Fe, Cu, sulfato, bicarbonato e outros
>ácidos 0.18% - cítrico,
fórmico, acético, láctico, oxálico
>enzimas - peroxidase, catalase,
fosfatase, lipase
>gases - oxigênio, nitrogênio e
CO 2
>vitaminas
O leite é uma mistura particularmente interessante. Pode ser
classificado como uma emulsão (de glóbulos de gordura
dispersos na fase aquosa) ou uma suspensão (de micelas de
caseína, proteínas globulares e partículas lipoprotéicas).
Além disso, a fase liquida é uma solução de lactose,
proteínas hidrossolúveis, minerais e outros componentes.
A gordura no leite

Algumas células das glândulas mamárias dos mamíferos
secretam gorduras - mais precisamente, triglicerídeos. Estas
células liberam pequenas "gotas" ou glóbulos de gordura que
são estabilizadas por uma cobertura lipo-protéica, derivada
da membrana plasmática das células excretoras. O leite
"integral", na verdade, não é integral. A legislação
brasileira determina uma quantidade mínima de gordura no
leite para esta classificação, e os fabricantes optam sempre
pelo mínimo, extraindo boa parte das gorduras e proteínas
excedentes, para a fabricação de derivados. Como é de origem
animal, a gordura láctea é predominantemente saturada
(>65%), contendo menos de 3% de gorduras poli-insaturadas.
Dentro destes glóbulos de gordura, existem moléculas
lipossolúveis muito importantes para o corpo humano:
vitamina A e colesterol, entre outras. Por isso o leite
desnatado é pouco nutritivo e quase não contém colesterol.
O consumo deste tipo de leite, infelizmente, vem aumentando
nos últimos anos no Brasil.

Dentre os ácidos graxos encontrados no leite, a maior parte
refere-se a ácidos de cadeia longa, como o o C16 palmítico
(26% da gordura), o C18:1 oléico (20%) e o C14 mirístico
(11%).
No leite de cabra, o acido C10 cáprico é também abundante,
conferindo o odor característico.
Proteinas no leite

O leite é rico em proteínas, de particularmente 3 tipos. A
mais abundante é a caseína - um complexo de várias unidades
protéicas, disperso na fase líquida do leite.
 Vários
fatores (como temperatura, pH e força iônica) podem provocar
a desnaturação da caseína, levando ao coalho do leite. No
leite coalhado, observa-se claramente a formação de duas
fases: uma sólida, que contém proteínas e gorduras, e outra
líquida (soro), que contém carbo-hidratos e água,
predominantemente. Vários
fatores (como temperatura, pH e força iônica) podem provocar
a desnaturação da caseína, levando ao coalho do leite. No
leite coalhado, observa-se claramente a formação de duas
fases: uma sólida, que contém proteínas e gorduras, e outra
líquida (soro), que contém carbo-hidratos e água,
predominantemente.
Lactose no leite

Dentre todos os carbo-hidratos encontrados no leite (O
QMCWEB já falou sobre carbo-hidratos). Esta molécula é um
dissacarídeo composta por uma unidade de glucose e outra de
galactose. Na maioria dos processos de produção de derivados
do leite, as bactérias convertem a lactose no ácido lático.
Quando deixamos o leite fora da geladeira, ele "azeda": este
fenômeno é justamente o resultado da fermentação do leite
pelas bactérias que produzem acido lático. A alteração do pH
do leite promove a coagulação de muitas de suas proteínas,
gerando a separação de fases.

No corpo humano, a lactose é quebrada por uma enzima chamada
lactase, em suas subunidades básicas. A glucose e a
galactose, então, são absorvidas pelo trato digestivo e
utilizadas no organismo.
Algumas pessoas sofrem deficiência de lactase; neste caso, o
leite se torna tóxico, na medida em que a lactose não pode
ser metabolizada, levando a males digestivos.
Vitaminas e minerais

O leite é uma excelente fonte de muitas vitaminas.
Entretanto, o leite pasteurizado já não possui muitas delas,
tal como a vitamina C, que é destruida durante este
processo. As vitaminas mais abundantes são a A e D, ambas
lipossolúveis. Muitos fabricantes, também, adicionam
quantidades extras destas vitaminas ao leite. O leite também
é uma fonte para o grupo B de vitaminas, principalmente para
a riboflavina, niacina e tiamina, além de traços de biotina,
piridoxina, ácido fólico e pantotênico.
Além de vitaminas, o leite contém também minerais, sendo uma
das mais importantes fontes de íons cálcio e fósforo em
nossa dieta. Também contém íons potássio, cloretos, sódio,
magnésio, cobre, iodetos e ferro. Muitos fabricantes
adicionam quantidades extras de alguns destes minerais,
sobretudo do ferro, no intuito de "fortificar" o leite.
|
Por que o leite derrama quando ferve?
|
Esta é uma das questões mais frequentes dos leitores
do QMCWEB. Finalmente, você poderá saciar a sua
dúvida.
Bem, começaremos a entender falando sobre a água.
Quando aquecemos um certo volume de água,
rapidamente observamos a liberação de bolhas de gás
- mesmo antes da fervura. Isto ocorre porque a
solubilidade dos gases diminui com o aumento da
temperatura (lei de Henry, lembra?). Menos solúveis,
os gases outrora dissolvidos formam bolhas e saem do
líquido.
No leite, entretanto, mesmo sob a forma de bolhas o
gás ainda fica "aprisionado" no líquido. O leite têm
uma série de substâncias capazes de estabilizar
estas bolhas, como a caseína. Com várias bolhas de
gás, o leite vai gradativamente aumentando de
volume. O gás se expande com o aumento da
temperatura, e então as bolhas ficam cada vez
maiores.
Próximo a fervura, entretanto, o volume destas
bolhas aumenta muito, as proteínas começam a se
desnaturar e a estabilidade do gás diminui
drasticamente. Ao mesmo tempo, ocorre uma separação
de fases: a camada de gordura fica sobre o líquido
da emulsão devido à desnaturação das caseínas. Esta
capa de gordura impede a saída imediata do gás que,
agora, já não é mais estabilizado. O fenômeno que
ocorre, então, é a escalada do líquido pelas paredes
do recipiente. E a meleca no fogão...
Você pode fazer em casa um experimento simples, que
prova que as micelas de caseína são as culpadas.
Tente ferver um pouco de leite após ter adicionado
algumas gotas de limão ou vinagre. A alteração no pH
provoca a desnaturação das proteínas do leite,
impedindo-as de estabilizarem as bolhas de gás. O
leite acidificado, então, passará a ferver como se
fosse água - sem derramar. Pena que o sabor não seja
muito agradável... |
Derivados do Leite
|
produto
100g
|
água
(g)
|
proteína
(g)
|
gordura
(g)
|
|
queijo
(Brie)
|
48
|
21
|
30
|
|
queijo
(Emmental)
|
37
|
28
|
27
|
|
sorvete
|
61
|
3.5
|
11
|
|
yogurt
|
85
|
5.3
|
3
|
|
manteiga
|
16
|
0.8
|
81
|
Fonte: Composition of Foods,
Agriculture Handbook no. 8-1, U.S. Department of Agriculture
|
|
 |