 Quando
João e Maria avistaram uma
casa feita de doces não resistiram: nem mesmo o medo da
bruxa malvada foi capaz de impedi-los de entrar. Todos
nós temos uma queda por doces:
poucos dispensam a sobremesa.
(A tara não se restringe aos humanos: o que pensar das
formigas?)
O Portal de Quando
João e Maria avistaram uma
casa feita de doces não resistiram: nem mesmo o medo da
bruxa malvada foi capaz de impedi-los de entrar. Todos
nós temos uma queda por doces:
poucos dispensam a sobremesa.
(A tara não se restringe aos humanos: o que pensar das
formigas?)
O Portal de
Estudos em Química apresenta os
açúcares e os compostos orgânicos não nutritivos
que estão sendo usados para "tapear" nosso paladar: os
adoçantes artificiais.
 O açúcar que utilizamos em casa contém a
sacarose: um dos
vários compostos orgânicos de sabor doce, incolores,
solúveis em água, encontrados na seiva de várias plantas
(como a cana-de-açúcar) e no leite de mamíferos. O açúcar
mais comum é justamente a sacarose, que, puro, é utilizado
na indústria de alimentos e bebidas.
O açúcar que utilizamos em casa contém a
sacarose: um dos
vários compostos orgânicos de sabor doce, incolores,
solúveis em água, encontrados na seiva de várias plantas
(como a cana-de-açúcar) e no leite de mamíferos. O açúcar
mais comum é justamente a sacarose, que, puro, é utilizado
na indústria de alimentos e bebidas.
Os açúcares pertencem a uma classe de compostos orgânicos
chamada carbohidratos*,
ou hidratos de carbono. O nome deriva da reação de
fotossíntese que ocorre nas plantas, com a ação catalítica
da clorofila: o dióxido de carbono se combina com a água
e formam a glucose. As moléculas de glucose podem se
combinar e formar outros dois componentes característicos
das plantas: a sacarose, a celulose e o amido. As
moléculas de celulose garantem a sustentação da planta, e as
de amido servem como um armazenamento de alimento para
servir à nova planta, durante o crescimento inicial.
Tanto a sacarose, amido ou celulose são vitais para as
necessidades básicas do homem. O Portal de Estudos em
Química, por exemplo, é uma das poucas revistas que não
utilizam celulose: todos os livros, jornais e revistas que
lemos são impressas em papel - feito de celulose. O pão
nosso de cada dia é feito com amido e adoçado com sacarose.
Mesmo a cervejinha gelada deve a sua existência à sacarose:
é a fermentação desta que produz o álcool e o CO2.
Nesta edição você ficará sabendo um pouco mais sobre os
carbohidratos.
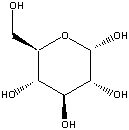
glucose
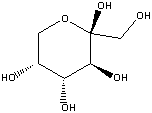
frutose
|
Os carbohidratos são, provavelmente, os compostos
orgânicos mais abundantes nos organismos vivos.
Estruturalmente, podem ser vistos como aldeídos
poli-hidroxilados ou cetonas polihidroxiladas; ou, ainda,
compostos que, pela hidrólise, podem se transformar nestes.
Eles podem sem divididos em quatro grandes grupos:
monossacarídeos, dissacarídeos, oligossacarídeos e
polissacarídeos. Os
monossacarídeos são os mais simples: apenas uma
unidade de açúcar em cada molécula. A glucose, a frutose e a
galactose são os monossacarídeos mais comuns, e possuem a
mesma fórmula molecular: C6H12O6.
A frutose e a glucose são encontradas em frutas e no mel e a
galactose no leite dos mamíferos. Embora tenham a mesma
fórmula molecular, estes compostos tem estruturas químicas
diferentes, isto é, são isômeros. O sabor de cada um também
é diferente. Sabe-se que o doce do açúcar depende
grandemente da posição dos grupos -OH que compõe a estrutura
molecular.
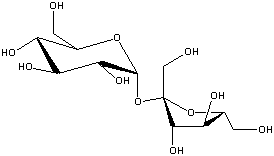 sacarose
sacarose
|
Quando duas moléculas de um açúcar simples se unem elas
formam um dissacarídeo.
A sacarose, por exemplo, é um dissacarídeo formado por uma
unidade de frutose e outra unidade de glucose. A energia
contida nas ligações químicas na frutose, glucose ou
sacarose é a resposável por suprir, na maioria dos seres
vivos, a energia necessária para suas atividades.
Os monossacarídeos podem, também, se combinar e formar
macromoléculas, com longas cadeias de unidades de frutose,
glucose ou galactose repetidas. Estes são os
polissacarídeos:
moléculas com mais de 10.000 unidades de açúcares. Mais de
uma centena de espécies foram identificadas, mas as mais
comuns são a celulose e o amido.
|
Proteínas
doces!
|
Dentre os novos compostos utilizados como adoçantes,
destacam-se duas proteínas: a monelna e a taumatina.
A monelina é uma
proteína heterodimérica com uma cadeia alfa de 45
amino-ácidos e outra cadeia beta de 50 amino-ácidos.
É isolada de uma planta africana que produz amoras,
a Dioscoreophyllum cumminsii diels.
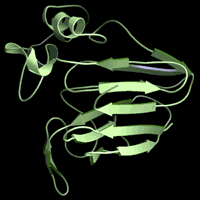
A taumatina é uma
proteína simples, com uma cadeia de 207 amino-ácidos.
É extraída do fruto da planta africana
Thaumatococcus daniellii benth. Ambas são cerca
de 3000 vezes mais doces do que a sacarose! Nós
conseguimos detectar a presença desta substância
mesmo em concentrações tão baixas como 1 x 10-8
M. Embora tenham também valor comercial, como
adoçantes, estas proteínas estão ajudando a entender
como os receptores sensoriais, na língua, funcionam.
|
Os carbohidratos são muito importantes para os seres vivos.
O mecanismo de
armazenamento de energia, para quase todos os
seres vivos de nosso planeta, baseia-se em carbohidratos ou
lipídeos - os carbohidratos são uma fonte de energia
imediata, enquanto que os lipídeos queimam em uma velocidade
menor, servindo para longo prazo. O ciclo metabólico da
glucose, por exemplo, é vital para os organismos vivos, tal
como o homem: falhas neste ciclo acarretam vários males, tal
como os desencadeados pela diabetes. Os seres ruminantes,
tal como o boi, são capazes de converter os polissacarídeos
como a celulose (indigesto para o homem) em açúcares
menores e proteínas; e são justamente estes seres a maior
fonte protéica para a humanidade. Vários antibióticos,
tal como a streptomicina, são derivados de carbohidratos. O
iogurte também deve sua existência aos carbohidratos: os
lactobacilos (bactérias que habitam o leite) convertem o
açúcar em ácido lático, gerando o iogurte.
A quantidade total de energia (ou, como a mídia normalmente
chama, "caloria") requerida para um indivíduo depende da
idade, ocupação e outros fatores, mas geralmente gira em
torno de 2.000 a 4.000 calorias (uma caloria, por definição,
é a quantidade de calor necessária para aumentar a
temperatura de 1,000 grama de água de 15o
para 16o C). Um grama de
carbohidrato produz cerca de 4 calorias, quando
metabolizado, no homem. Para efeito de comparação, um grama
de gordura produz cerca de 9 calorias e 1 grama de proteína
produz também 4 calorias. Como são rapidamente metabolizados
e altamente energéticos, os carbohidratos são, geralmente,
os pratos principais dos atletas antes das competições.
Esta alta capacidade calórica pode ser, para alguns,
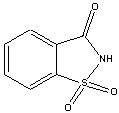 sacarina
sacarina
|
um problema: muitas pessoas, por motivo de saúde ou
estética, precisam evitar o consumo de açúcar. Um bolo
amargo ou um refrigerante salgado não agradaria ninguém: é
aí que entram os químicos e os adoçantes artificiais. O
primeiro composto químicos a ser utilizado como um
substitutivo da sacarose foi a
sacarina (a imida
do ácido orto-sulfobenzóico). Em 1879, os químicos Ira
Remnsen e Constantin Fahlberg, investigavam a oxidação do
o-toluenosulfonamida. Após uma tarde exaustiva de trabalho,
foram para a lanchonete, onde perceberam que os seus lanches
estavam estupidamente doces! Fahlberg lembrou que não havia
lavado as mãos ao sair do laboratório; checando os produtos
da reação, ele descobriu a sacarina, um composto orgânico
cerca de 500 vezes mais doce que o açúcar. O composto
parecia perfeito: muito solúvel em água e, pásmem!, não era
metabolizado pelo organismo: amostras de urina revelaram que
o composto saia intacto do organismo. Diabéticos e pessoas
que não querem ganhar peso rapidamente adotaram a sacarina
como adoçante. Hoje, vários produtos alimentícios "diet"
utilizam a sacarina para dar o sabor doce, sem nenhum valor
calórico. Embora alguns estudos tenham evidenciado o aumento
de câncer no fígado e nos rins, em ratos, o consumo de
sacarina foi aprovado e estimulado na grande maioria dos
países.
Outros adoçantes artificias vieram logo em seguida. Um deles
foi o ciclamato
(ácido N-Ciclohexilsulfâmico) ou derivados,
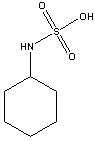 clclamato
clclamato
|
que são cerca de 30 vezes mais doces que a sacarose. São
muito usados em bolos, doces, refrigerantes e como
conservantes na indústria alimentícia. Foram descobertos em
1937, por Michael Sveda. Tal como a sacarina, não possuem
valor calórico, pois não são metabolizados no organismo
humano. Entretanto, algumas bactérias presentes no trato
intestinal podem hidrolizar os ciclamatos para formar a
ciclohexilamina, um potencial carcinogênico. Dois estudos
científicos, feitos na década de 70, associaram a ingestão
de ciclamatos com câncer nos rins em ratos. Embora seja
proibido nos Estados Unidos, o ciclamato é utilizado em
vários países, incluindo o Brasil.
 Embora
recente, o aspartame
já é um dos adoçantes mais utilizados e mais
polêmicos. Devido ao seu grande consumo, várias indústrias
açucareiras espalharam na mídia e na internet uma boataria
sobre "os grandes males" provocados pelo aspartame. Centenas
de spams, via e-mail, chegam até hoje, à redação do QMCWEB,
alertando para os "perigos" do aspartame. Na internet,
milhares de sites dedicam-se exclusivamente a incentivar o
boicote do aspartame. Sem nenhum fundamento científico,
estes boatos visam denegrir a imagem deste adoçante que pode
comprometer os lucros das usinas de açúcar. Embora
recente, o aspartame
já é um dos adoçantes mais utilizados e mais
polêmicos. Devido ao seu grande consumo, várias indústrias
açucareiras espalharam na mídia e na internet uma boataria
sobre "os grandes males" provocados pelo aspartame. Centenas
de spams, via e-mail, chegam até hoje, à redação do QMCWEB,
alertando para os "perigos" do aspartame. Na internet,
milhares de sites dedicam-se exclusivamente a incentivar o
boicote do aspartame. Sem nenhum fundamento científico,
estes boatos visam denegrir a imagem deste adoçante que pode
comprometer os lucros das usinas de açúcar.
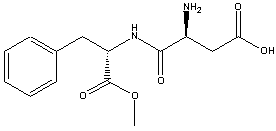 aspartame
aspartame
|
O aspartame, ou aspartilfenilalanina, foi descoberto
em 1965. Ao contrário dos anteriores, o aspartame tem um
certo valor (irrisório) calórico. Mas, como é cerca de 150
vezes mais doce do que a sacarose, a quantidade utilizada em
um prato é muito pequena e, por consequência, não causa
nenhuma contribuição nutricional. É, atualmente, o adoçante
preferido pelos fabricantes de refrigerantes e outros
produtos alimentícios. É totalmente contra-indicado aos que
sofrem de uma doença rara: os fenilcetonúricos (por isso, na
"Coca-Light", existe um aviso a respeito).
|
Cerveja... light ?!
|
|
Embora os refrigerantes possam ser fabricados com
adoçantes artificiais não nutritivos, isto não pode
ser feito com bebidas alcóolicas. No processo de
fabricação, enzimas presente no fermento convertem a
glucose em etanol e gás carbônico. Como os adoçantes
artificiais não contém glucose, não podem substituir
o açúcar nas bebidas alcóolicas. Neste caso, a
melhor estratégia é beber algo bastante forte, onde
a maioria da glucose já foi convertida para o
etanol! |
Mais recentemente, vários compostos foram adicionados à
lista dos adoçantes artificiais.
 Entre
estes, a Taumatina, uma proteína extraída da planta africana
Thaumatococcus Danielli, que já utilizado no Japão
desde 1979 (vide quadro acima). O acesulfame de potássio
(vendido como Sunette) foi aprovado no EUA em 1988. A
steviosida, derivada da planta
Stevia Rebaudiana,
foi usada no Japão e, hoje, está sendo utilizada em países
da América do Sul, tal como no Brasil: é cerca de 300 vezes
mais doce do que a sacarose. Em 1981, foi patenteado, nos
EUA, a L-sacarose. Para olhos destreinados, a estrutura
molecular da L-sacarose parece idêntica a da sacarose. Este
composto, entretanto, é a imagem especular (um
estereoisômero) da sacarose que utilizamos. Enquanto que
esta é metabolizada pelo organismo, a L-sacarose, embora
doce, é excretada intacta - não é reconhecida pelos sítios
catalíticos metabólicos. O único problema é a fabricação:
enquanto que a D-sacarose é facilmente extraída da
cana-de-açúcar, a L-sacarose é sintética e o processo é caro
e demorado. Entre
estes, a Taumatina, uma proteína extraída da planta africana
Thaumatococcus Danielli, que já utilizado no Japão
desde 1979 (vide quadro acima). O acesulfame de potássio
(vendido como Sunette) foi aprovado no EUA em 1988. A
steviosida, derivada da planta
Stevia Rebaudiana,
foi usada no Japão e, hoje, está sendo utilizada em países
da América do Sul, tal como no Brasil: é cerca de 300 vezes
mais doce do que a sacarose. Em 1981, foi patenteado, nos
EUA, a L-sacarose. Para olhos destreinados, a estrutura
molecular da L-sacarose parece idêntica a da sacarose. Este
composto, entretanto, é a imagem especular (um
estereoisômero) da sacarose que utilizamos. Enquanto que
esta é metabolizada pelo organismo, a L-sacarose, embora
doce, é excretada intacta - não é reconhecida pelos sítios
catalíticos metabólicos. O único problema é a fabricação:
enquanto que a D-sacarose é facilmente extraída da
cana-de-açúcar, a L-sacarose é sintética e o processo é caro
e demorado.
A idéia é simples: conseguir o sabor doce sem a injeção
calórica da sacarose e, principalmente, sem efeitos
colaterais no organismo. Químicos do mundo inteiro continuam
a busca por mais substâncias com estas propriedades:
moléculas doces!

*
= Os
dicionários da língua portuguesa, tal como o
Aurélio, escrevem "carboidratos", sem o "h".
Achamos a forma "carbohidrato" mais correta,
pois o nome vem da combinação "hidrato" +
"carbono". O "h", neste caso, tem a mesma função
desempenhada em palavras como "hidráulico" ou
"hidroginástica". O "h", embora não pronunciado,
denota a presença de um elemento químico - o
hidrogênio. Para o editor do QMCWEB, os
dicionários é que estão equivocados. Ainda, o
termo em inglês é "carbohydrate". Este não é o
único exemplo de termo científico "erronemente
traduzido" para o português...
|
|
|