 INTRODUÇÃO
INTRODUÇÃO
|
Dentre
todas as substâncias químicas,
uma das mais conhecidas e
estudadas é o benzeno. Formada por apenas 12
átomos - 6 carbonos e seis hidrogênios, esta molécula figura
em qualquer livro de química. A maior parte das
substâncias com atividade biológica apresentam, em sua
estrutura, o anel benzênico, assim como os alcalóides,
alguns amino ácidos e muitos polímeros sintéticos. Em várias
ocasiões, a molécula do benzeno esteve presente também no
Portal de Estudos em Química.
 A molécula de benzeno descrita pela
teoria da ligação de valência. Os
carbonos sp2
híbridos formam ligações
s
com seus vizinhos e os orbitais p não
hibridizados se sobrepõe para formar
ligações p.
O padrão corresponde ao previsto por
Kekulé.
A molécula de benzeno descrita pela
teoria da ligação de valência. Os
carbonos sp2
híbridos formam ligações
s
com seus vizinhos e os orbitais p não
hibridizados se sobrepõe para formar
ligações p.
O padrão corresponde ao previsto por
Kekulé.
|
|
A molécula dos sonhos
|
 A
estrutura cíclica do benzeno foi desvendada
em um sonho. Mesmo após a fórmula molecular
do benzeno ser conhecida, não se tinha
nenhuma informação sobre a sua fórmula
estrutural. Aparentemente, a proporção entre
H/C parecia estar equivocada. A
estrutura cíclica do benzeno foi desvendada
em um sonho. Mesmo após a fórmula molecular
do benzeno ser conhecida, não se tinha
nenhuma informação sobre a sua fórmula
estrutural. Aparentemente, a proporção entre
H/C parecia estar equivocada.
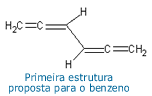 por Josef Loschmidt, em 1850
por Josef Loschmidt, em 1850
|
Em 1865, Friederich
Kekulé, um químico alemão já
reconhecido por seu trabalho na química
orgânica estrutural, cochilou na sua cadeira
enquanto estava intrigado com a estrutura do
benzeno. Então teve um sonho, sobre uma
serpente que mordia a própria cauda. Desta
idéia surgiu a primeira estrutura cíclica da
química - o anel benzênico.
Segundo suas próprias anotações: "I
turned my chair to the fire (after having
worked on the problem for some time) and
dozed. Again the atoms were gamboling before
my eyes. This time the smaller groups kept
modestly to the background. My mental eye,
rendered more acute by repeated vision of
this kind, could not distinguish larger
structures, of manifold conformation; long
rows, sometimes more closely fitted together;
all twining and twisting in snakelike motion.
But look! What was that? One of the snakes
had seized hold of its own tail, and the
form whirled mockingly before my eyes. As if
by a flash of lighting I awoke... Let us
learn to dream, gentlemen.
" |
|

|
Biografia
|
 Michael
Faraday
(1791-1867) nasceu na Inglaterra, muito pobre. Com
14 anos, começou a trabalhar como encadernador em
uma biblioteca, e educou a si mesmo lendo os livros
no tempo ocioso. Em 1833, tornou-se um professor de
química na Royal Institution. Ficou famoso com seu
trabalho com eletroquímica. Michael
Faraday
(1791-1867) nasceu na Inglaterra, muito pobre. Com
14 anos, começou a trabalhar como encadernador em
uma biblioteca, e educou a si mesmo lendo os livros
no tempo ocioso. Em 1833, tornou-se um professor de
química na Royal Institution. Ficou famoso com seu
trabalho com eletroquímica.

 Eilhardt
Mitscherlich (1794-1863) nasceu na
Alemanha. Seu sonho sempre foi o de acompanhar uma
delegação de Napoleão para a Pérsia; para tanto,
chegou a aprender o idioma. Com a derrota de
Napoleão, voltou para Berlin, onde se tornou um
professor de Química na University of Berlin. Eilhardt
Mitscherlich (1794-1863) nasceu na
Alemanha. Seu sonho sempre foi o de acompanhar uma
delegação de Napoleão para a Pérsia; para tanto,
chegou a aprender o idioma. Com a derrota de
Napoleão, voltou para Berlin, onde se tornou um
professor de Química na University of Berlin.
|
O composto que conhecemos como benzeno foi isolado pela
primeira vez em 1825, por
Michael Faraday. Ele extraiu o composto de um gás
obtido do óleo de baleia, que era utilizado para a
iluminação pública em Londres. Devido a sua origem, os
químicos da época sugeriram o nome "feno", da palavra
grega "phainei" (brilhar). Em muitos compostos, o
nome feno continua associado com o anel benzênico, tal como
no fenol. Somente nove anos depois (1834) é que a fórmula
molecular (C6H6)
foi corretamente determinada, por
Eilhardt Mitscherlich.
Ele decidiu chamar o composto de benzina, devido a sua
relação com o ácido benzóico, um composto conhecido na
época. Finalmente, mais tarde, o nome passou a ser
benzeno.
 |
|
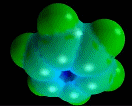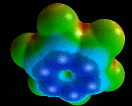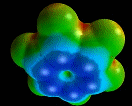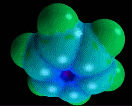
Elétrons p
|
No benzeno e em outros compostos similares, a relação H/C é
bastante baixa. Estes compostos são tipicamente encontrados
em óleos produzidos por plantas. Os químicos antigos
chamavam estes compostos de "aromáticos",
devido ao agradável aroma que, em geral, estas substâncias
possuem. Desta forma, eles eram distinguidos dos "alifáticos",
compostos onde a relação H/C é bem mais alta, que são
obtidos, por exemplo, na degradação química de gorduras.
Hoje, o termo aromático tem outro significado químico:
identifica certos tipos de estruturas, sem levar em conta a
presença ou não de odor. Para ser aromático, o composto deve
ser cíclico, planar, e deve possuir uma nuvem contínua de
elétrons pi deslocalizados, e a nuvem deve conter um número
par de pares de elétrons pi. O benzeno é um composto
aromático, baseado nos critérios atuais.
|
|