







|
|
BIOQUÍMICA
Hidratos de carbono, lipídios e
proteínas
- Hidratos de carbono
- Lipídios
- Proteínas

Hidratos de carbono (carboidratos, açúcares, glúcides,
glicídios)
Os hidratos de carbono são considerados compostos de função
mista poliálcool-aldeído ou poliálcool-cetona, formando os
referidos compostos de função mista.
Fórmula geral:
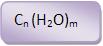
Exemplos:
Glicose: C6H12O6 ou C6(H2O)6
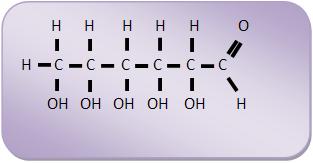
Frutose: C6H12O6
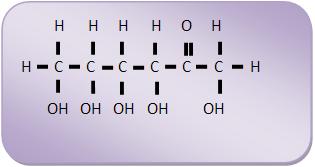
Monossacarídeos ou oses
- São os polidroxialdeídos (aldoses) e as polidroxi-cetonas (cetoses).
São os açúcares não-hidrolisáveis.
Exemplos: glicose (aldoexose) e frutose (cetoexose).
Subdividem-se em:
Aldoses: todos que
apresentam o grupo aldeídico.
Conforme o número de átomos de C classifica-se em
aldotriose (3C);
aldotetrose (4C) etc.
Cetoses: todos que
apresentam o grupo cetônico. Classificam-se também em
cetotriose,
cetotetrose etc.
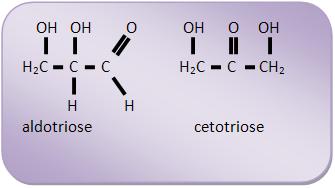
Exemplos de monossacarídeos
Glicose
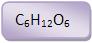
(glucose, dextrose, açúcar de uva)
a) Ocorrência
A glicose é encontrada no mel e frutos doces
(principalmente uva).
b) Obtenção
Hidrólise do amido em meio ácido:
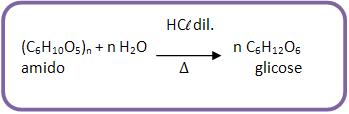
c) Aplicações
1) Fabricação de álcool etílico.
2) Alimentação de crianças, de atletas (após as
competições).
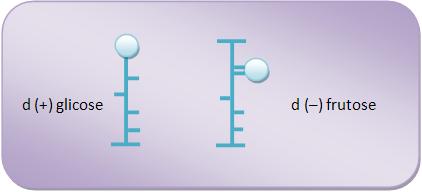
Frutose

(levulose)
A frutose também é encontrada no mel, nos frutos
doces, mas sempre na forma dextrogira ou d (–).
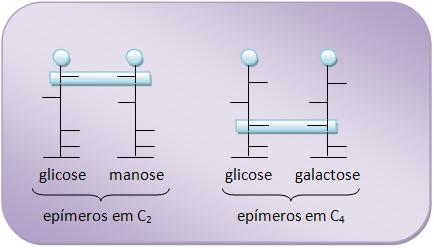
Oses epímeras
São oses que apresentam uma diferença na configuração de
um único carbono assimétrico.
Vejamos o exemplo abaixo:
• Glicose e manose são epímeros em C 2.
• Glicose e galactose são epímeros em C 4.
Simplificação das fórmulas
estruturais das oses
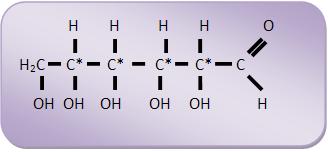
Normalmente representa-se as fórmulas das aldoses e cetoses na
vertical. Na fórmula, uma bola pode representar o grupo aldeído,
o sinal = O representa o grupo cetona, um traço o grupo
hidroxila e uma linha vertical a cadeia principal.
Isomeria nos açúcares
Quando uma aldose apresenta n átomos de carbono, ela irá
possuir (n - 2) átomos de carbono assimétricos e
diferentes, ou seja, 2n-2 isômeros
opticamente ativos.
Quando uma Cetose apresenta n átomos de carbono, ela irá
possuir (n – 3) átomos de carbono assimétricos e
diferentes, ou seja, 2n-3 isômeros
opticamente ativos.
É possível uma cetoexose possuir 3 carbonos assimétricos
diferentes. Portanto podemos concluir que também é
possível oito isômeros, onde destes oito isômeros apenas
a frutose será “farta” na natureza.
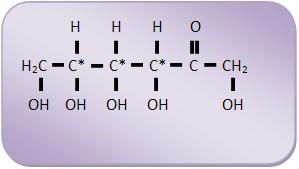
É possível uma aldoexose possuir 4 carbonos
assimétricos diferentes. Portanto podemos concluir que
também são possíveis 16 isômeros, onde destes 16
isômeros apenas três serão abundantes na natureza: a
glicose, a galactose a manose.
Osídeos - São os
açúcares hidrolisáveis. Podem ser dissacarídeos (sacarose, lactose, maltose,
celobiose, etc.) ou polissacarídeos (amido, glicogênio e celulose)
Eles se classificam em:
1) Holosídeos:
Holosídeos são osídeos, que através da hidrólise fornecem oses.
Eles se subdividem em:
Dissacáridos (dissacarídeos):
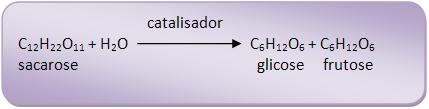
Dissacáridos (dissacarídeos) são os açúcares que se hidrolisam,
fornecendo duas moléculas de monossacáridos.
Vejamos o exemplo:
Sacarose, maltose, de fórmula C 12H 22O 11
Polissacáridos:
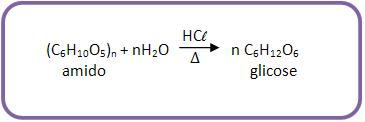
Polissacáridos são os açúcares que se hidrolisam, originando
mais de duas moléculas de monossacáridos.
Vejamos o exemplo:
Amido, celulose, de fórmula (C6H10O5)n.
2) Heterosídeos:
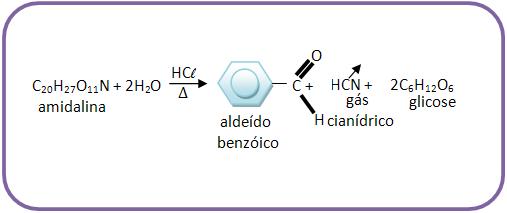
Heterosídeos são osídeos, que através da hidrólise fornece tanto
as oses como outros compostos.
Vejamos o exemplo:
Amidalina (semente de amêndoas amargas)
Dissacarídeos
| C12H22O11
|
+ H2O ®
|
C6H12O6
|
+
|
C6H12O6
|
sacarose
lactose
maltose
celobiose |
|
glicose
glicose
a glicose
b glicose
|
|
frutose
galactose
a glicose
b glicose |
Exemplo de dissacarideos:
Sacarose

(açúcar da cana, açúcar comum)
a) Ocorrência
A sacarose é muito encontrada em plantas, mas em especial na
cana–de–açúcar e na beterraba.
b) Obtenção
Vejamos a seguinte seqüência:
1) Obtenção da garapa.
2) Precipitação das proteínas e ácidos livres
através do tratamento com hidróxido de cálcio.
3) Eliminação do excesso de Ca(OH)2,
borbulhando CO2 (precipita CaCO3).
4) Filtração e cristalização através da
centrifugação, separando o melaço do açúcar.
c) Constituição
A sacarose é o resultado da condensação de α – glicose –
piranose com β – frutose – furanose através dos grupos (OH)
glicosídicos de cada uma.
d) Propriedades
Dentro das propriedades, a sacarose não diminui o licor de
Fehling, pelo fato de não haver um grupo aldeídico potencial ou
livre.
É importante sabermos que a sacarose se cristaliza facilmente e
não apresenta mutarrotação.
Polissacarídeos
| (C6H10O5)n
|
+ nH2O ®
|
nC6H12O6
|
amido
celulose
glicogênio |
|
a glicose
b glicose
a glicose |
Exemplo de polissacarídeos
Celulose
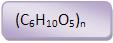
a) Ocorrência:
A celulose é encontrada em todos os vegetais, mas em especial no
algodão que possuí 95% de celulose.
b) Constituição:
A celulose é resultado da condensação de moléculas de
β–glicose.
A celulose possui uma massa molecular média da ordem de
400.000u, o que faz com que se torne indigerível pelo organismo
humano.
c) Aplicação:
1) Fabricação do papel, tecidos de algodão.
2) Preparação do algodão – pólvora (pólvora sem
fumaça), explosivo potente. É o tinitrato de celulose, obtido
pela esterificação das 3 oxidrilas para cada 6 átomos de carbono
com mistura sulfonítrica.
3) Preparação das piroxilinas (mono e dinitrato
de celulose), utilização na fabricação de celulóide, filmes,
linhos, sedas artificiais.
4) Fabricação de vidros de segurança para
carros.
Amido

a) Ocorrência
O amido está presente na substância de reserva dos
vegetais.
b) Constituição
O amido é resultado da condensação de moléculas de α
– glicose.
c) Aplicações
1) Alimentação
2) Fabricação de cola, da glicose
(hidrólise) e álcool etílico.
3) Na iodometria, a solução de
amido aparece como indicador. Adquire com o iodo uma
coloração violeta, que desaparece com sofre
aquecimento, mas a coloração volta quando houver
resfriamento.
O glicogênio é o amido animal, formado no fígado,
pela condensação de moléculas de glicose, queimando
as exigências metabólicas.
Lipídios são substâncias que, por hidrólise,
fornecem ácido(s) graxo(s) (obrigatoriamente), ao lado de outros compostos.
Podem ser glicerídeos, cerídeos, fosfolipídios e cerebrosídios.
Glicerídeos são ésteres do glicerol com ácidos
graxos. Os óleos e gorduras são misturas de glicerídeos.
Nas gorduras, predominam glicerídeos de ácidos saturados
(palmítico e esteárico) e são "sólidas" à temperatura ambiente.
Nos óleos, predominam glicerídeos de ácidos insaturados (oleico)
e são líquidos à temperatura ambiente.
Características dos lipídeos
A) Brancos ou levemente amarelados.
B) Gorduroso ao tato.
C) Pouco consistentes, podendo ser líquidos.
D) Sobre o papel, deixam uma mancha translúcida
que não desaparece por aquecimento.
E) Insolúveis na água.
Ácidos graxos mais comuns
C15H31-COOH
palmítico
C17H35-COOH
esteárico
C17H33-COOH
oleico (uma =)
Classificação dos lipídeos
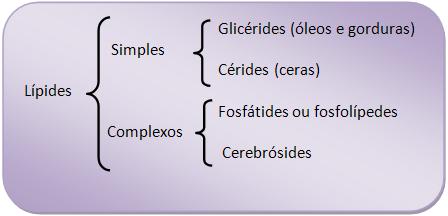
Cerídeos são ésteres de ácidos graxos e álcoois
superiores. Entram na constituição das ceras (cera de abelha, cera de
carnaúba, etc.).
Fosfatídios ou fosfolipídios são ésteres do
glicerol com ácidos graxos, H3PO4 e aminoálcoois.
Exemplos: lecitinas e cefalinas.
Cerebrosídios são ésteres de ácidos graxos com
galactose e aminoálcoois.
Principais óleos e gorduras
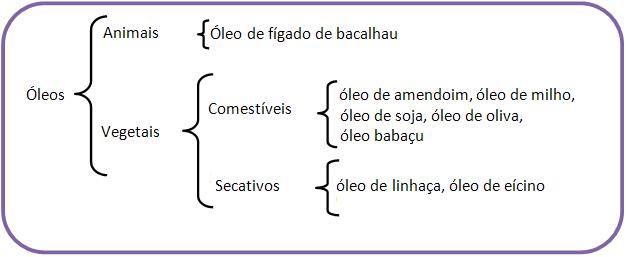

Propriedades dos óleos e gorduras
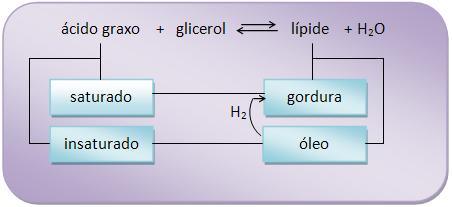
A) Hidrólise e
saponificação
A formação de uma triglicéride é uma reação de
esterificação, podendo se tornar reversível.
A hidrólise sendo feita no meio ácido de uma gordura ou
de um óleo, forma-se o glicerol e uma mistura de ácidos
carboxílicos, podendo assim ser separados por destilação
fracionada.
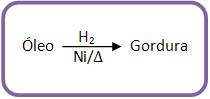
B) Transformação de óleo
em gordura
Com a hidrogenação do óleo na presença de níquel a 150°
C, todos os glicéridos insaturados ficam saturados,
tornando-se sólido, ou seja, o óleo é transformado em
gordura.
Observação: se os óleos vegetais forem
hidrogenados, irá obter a margarina.
C) Rancificação de
óleos e gorduras
Rancificação é considerada uma transformação química
complexa, formada de hidrólises e oxidações. Dentro do
processo químico, obtem-se compostos que deixam o
produto com cheiros desagradáveis.
Índice de saponificação
Esse índice é considerado a massa de KOH, dado
em miligrama, que é necessária para que ocorra a
saponificação de um grama de óleo ou gordura.
Índice de iodo
Índice de iodo é a massa do iodo em
gramas que é adicionada por 100g de
glicéride.
Definição
Proteínas são substâncias formadas por
macromoléculas resultantes da condensação de grande número de moléculas de
a aminoácidos carboxílicos.
Na cadeia peptídica, os aminoácidos estão unidos por
ligações peptídicas.
Aminoácidos essenciais -
Não são elaborados pelo organismo e, por isso, devem ser introduzidos sob a
forma de alimentos.
Exemplos: Glicina, Alanina e cisteína.
Caráter anfótero
Por apresentarem um grupo ácido e outro básico, os aminoácidos
reagem tanto com as bases minerais como com os ácidos minerais.
Eles se apresentam na forma de sais, pelo fato de haver uma
neutralização intramolecular, este fato explica o estado sólido
dos aminoácidos e a solubilidade em água.
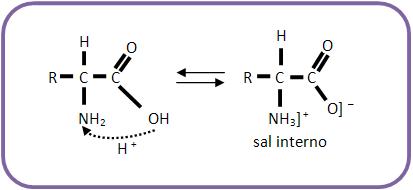
O resultado é um íon dipolar que apresenta um
momento dipolar elevado, denominado
zwitterion.
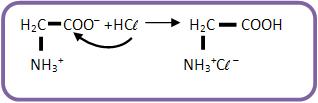
Reação com ácido:
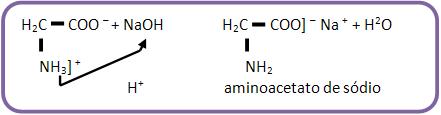
Reação com base:
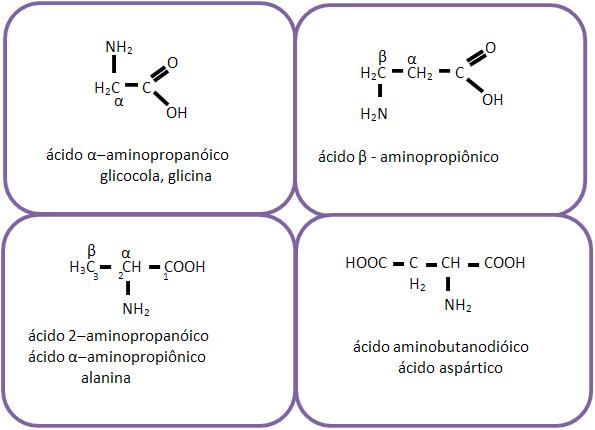
Classificação e nomenclatura
dos aminoácidos
A classificação e a nomenclatura dos aminoácidos variam
conforme a posição do grupo amino, como por exemplo: α,
β, γ etc.
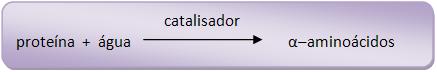
Hidrólise das proteínas
A hidrólise das proteínas ocorre no processo de
aquecimento prolongado de uma proteína na
presença de ácido forte ou base forte diluídos
formando assim α–aminoácidos. A hidrólise
catalítica ocorre no organismo humano, ocorrendo
pela ação das enzimas como pepsina do suco
gástrico.
Estrutura das Proteínas
 | Primária
É constituída pela sequência dos aminoácidos.
Uma proteína por convenção é considerada um
polipeptídio que contêm massa molecular acima de 10.000u. Uma proteína é
considerada uma poliamida, contendo resíduos de aminoácidos, que ficam
ligados uns aos outros através da ligação amida.
O grupo amida:

A sequência dos resíduos de aminoácidos na cadeia peptídica é chamada de
estrutura primária.
Com os aminoácidos glicina e alanina são possíveis dois dipeptídeos
diferentes.
|
 |
Secundária
Resulta da interação da estrutura primária com ela mesma, através da
formação de pontes de hidrogênio. Pode ser em forma de hélice
a ou de folha pregueada.
|
 |
Terciária
É a forma tridimensional da proteína, ocasionada pelo enrolamento das
cadeias peptídicas sob a forma de novelo. |
Desnaturação - É a
perda da ação biológica da proteína causada por aquecimento ou variação do
pH. Resulta da destruição da estrutura terciária.
Classificação das Proteínas pelo seu papel biológico
As proteínas de construção, como o nome indica,
são as responsáveis pela construção dos tecidos. São também chamadas
proteínas estruturais.
Exemplos:
 | Colágeno
Presente nos ossos, cartilagens, tendões e também na pele.
|
 |
Queratina
É a mais abundante dos pêlos (inclusive cabelos) e unhas.
|
 |
Miosina
Principal constituinte dos músculos e responsável pela contratilidade. |
 | Albumina
Proteína mais abundante no plasma sanguíneo.
|
 |
Hemoglobina
Presente nas hemácias e importante no transporte de oxigênio pelas
células vermelhas.
As proteínas de catálise são as enzimas. São
os catalisadores das reações enzimáticas.
Exemplos:
|
 |
Amilase
Catalisa a hidrólise do amido até a maltose. |
 | Maltase
Catalisa a hidrólise da maltose até glicose.
|
 |
Pepsina
Catalisa a hidrólise das proteínas no estômago.
As proteínas de defesa são os anticorpos
produzidos por células específicas do sistema imunológico, chamada
linfócitos.
A capacidade do nosso organismo de repelir a infecção
depende inteiramente de alguns órgãos e tecidos específicos, como o
timo, o baço, os gânglios linfáticos e a medula óssea.
São exemplos de anticorpos:
|
 |
Antitoxinas
Neutralizam as toxinas dos agentes de infecção, como as bactérias. |
 | Aglutininas
Aglutinam certos agentes de infecção.
|
 |
Opsoninas
Tornam os agentes de infecção mais facilmente atacáveis pelos fagócitos.
|
 |
Lisinas
Dissolvem certos agentes de infecção. |
Home | Histórico | Classificação das Cadeias Carbônicas | Funções Orgânicas | Nomenclatura | Polímeros | Reações Orgânicas | Propriedades Físicas dos Compostos Orgânicos | Petróleo | Isomeria | Bioquímica
Este site foi atualizado em
04/03/19
|

